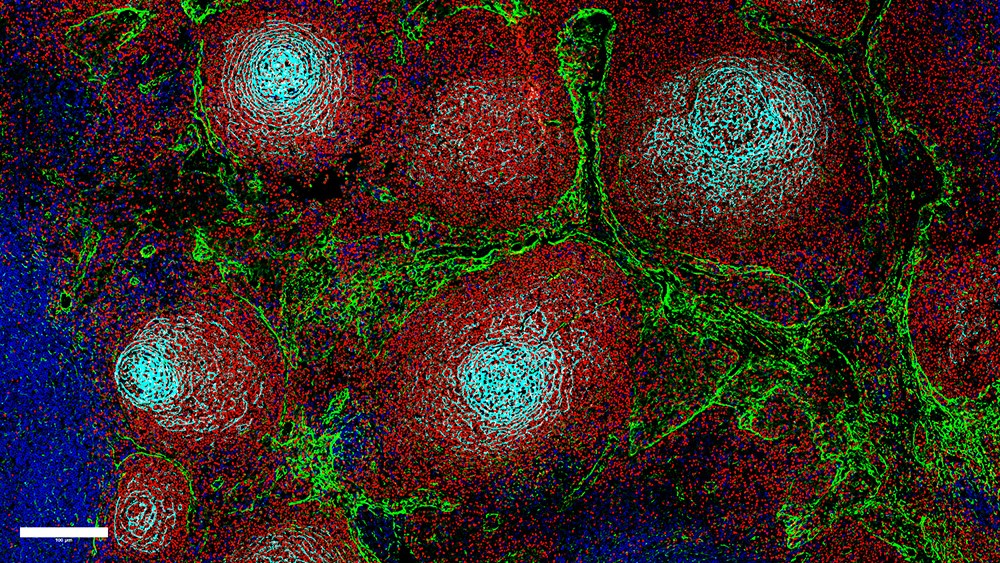
High-throughput testing of drugs on mini-tumors reveals vulnerabilities in meningiomas
Meningiomas are the most common brain tumors. Until now, only two methods have generally been considered for treating them: surgery and radiation therapy. A research team in Heidelberg has now developed a potential new approach for effective systemic therapy. Its members from Heidelberg University’s Faculty of Medicine and Heidelberg University Hospital (UKHD) tested the effectiveness of drugs against meningiomas. Among other things, they used so-called organoids—mini-tumors created in the lab whose cell composition closely matched that of patient tumors. In doing so, they discovered that the drug panobinostat can be effective against aggressive meningiomas. In the event that the tumor becomes resistant to the active ingredient, the researchers also found a solution through the targeted inhibition of the enzyme HDAC8.
Full text in German below.
Hochdurchsatz-Tests von Wirkstoffen an Mini-Tumoren zeigen Schwachstellen von Meningeomen
Meningeome sind die häufigsten Tumoren des Gehirns. Um sie zu bekämpfen, kommen bisher meist nur zwei Methoden in Frage: Operation sowie Bestrahlung. Einen möglichen neuen Ansatz für eine wirksame systemische Therapie hat jetzt ein Heidelberger Forschungsteam entwickelt. Seine Mitglieder von der Medizinischen Fakultät Heidelberg der Universität Heidelberg und vom Universitätsklinikum Heidelberg (UKHD) testeten die Wirksamkeit von Medikamenten gegen Meningeome. Unter anderem setzten sie sogenannte Organoide ein, im Labor erzeugte Mini-Tumoren, deren Zell-Zusammensetzung fast genau den Patienten-Tumoren entsprach. Dabei fanden sie heraus, dass das Medikament Panobinostat gegen aggressive Meningeome wirken kann. Für den Fall, dass der Tumor gegen den Wirkstoff resistent wird, fanden die Forschenden außerdem Abhilfe durch die gezielte Hemmung des Enzyms HDAC8.
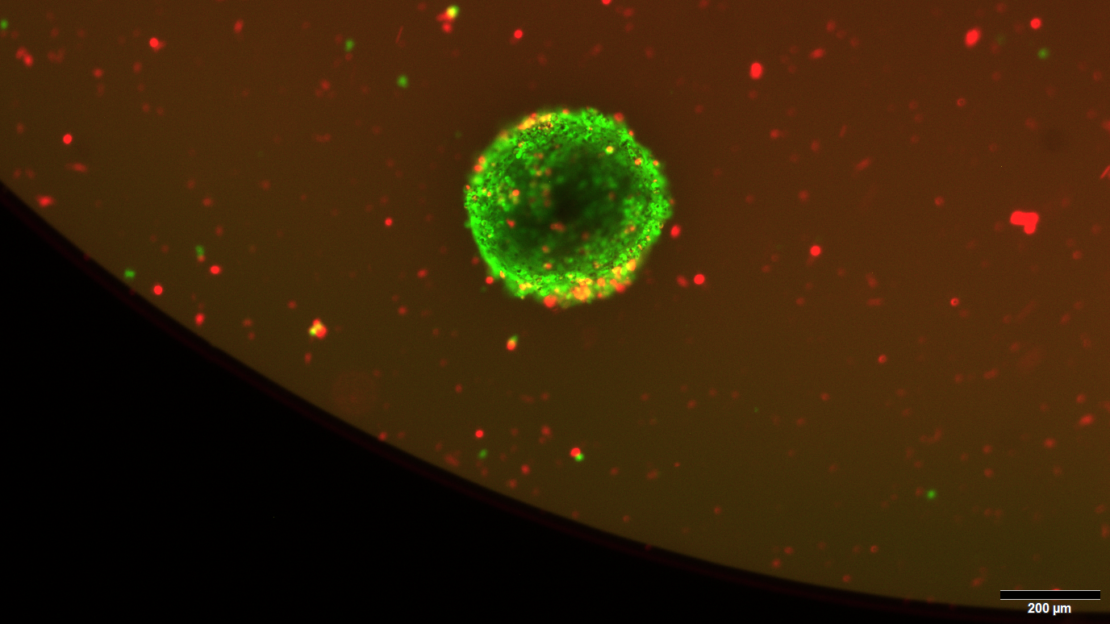
Ziel der Forscherinnen und Forscher war es, einen neuen Therapieansatz gegen Meningeome zu entwickeln und so eine Lücke der verfügbaren Behandlungsmethoden zu schließen. Dazu nutzten sie in einem ersten Schritt Zelllinien der Meningeome, die sie zum Teil im eigenen Labor entwickelten. Zelllinien sind aus dem Hirntumor entnommene Zellen, die im Labor langfristig vermehrt werden. Bei einem Screening von 107 verschiedenen Krebsmedikamenten konnten die Forschenden neun vielversprechende Hemmstoffe, sogenannte Inhibitoren identifizieren.
Organoide bilden echte Tumoren fast identisch ab
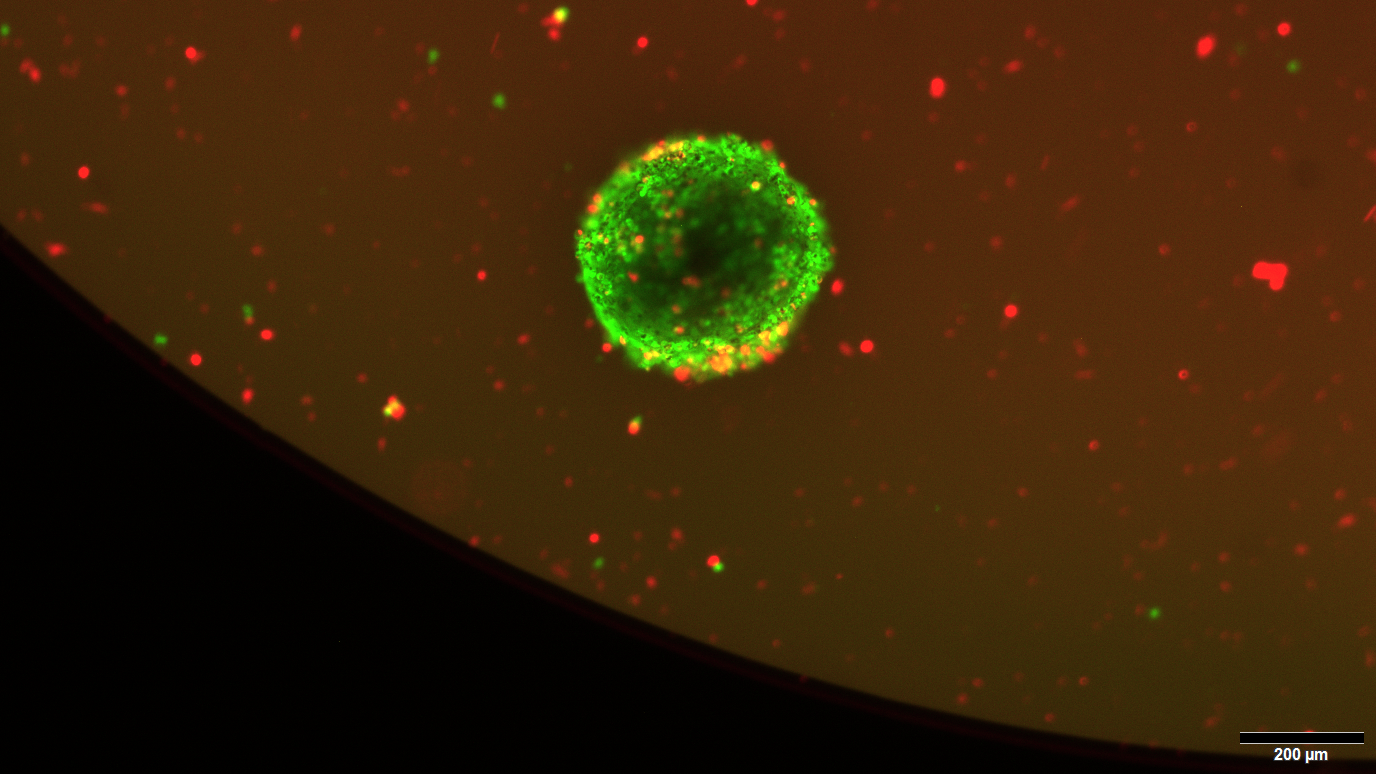
Im zweiten Schritt überprüfte die Arbeitsgruppe die neun potenziell wirksamsten Medikamente anhand von standardisierten Organoid-Modellen, die den echten Tumor nahezu identisch im Labor nachbilden. „Diese Mini-Tumoren sind Kurzzeitsysteme, die die zelluläre Komplexität des Patiententumors exakt widerspiegeln. Sie enthalten unter anderem auch Nicht-Tumorzellen, die im echten Meningeom vorkommen und einen Einfluss auf die Medikamentenwirksamkeit haben können. Außerdem stimmen sie in den genetischen Veränderungen und der charakteristischen Genaktivität überein“, erläutert Prof. Dr. Christel Herold-Mende, die die Sektion Neurochirurgische Forschung des Universitätsklinikums Heidelberg leitet.
Das Verfahren zur Testung von Medikamenten hat ihre Arbeitsgruppe mit der Plattform namens HeiDePEx standardisiert. Über HeiDePEx lassen sich innerhalb weniger Tage Medikamente am Organoid testen: Nachdem das Operations-Team der Neurochirurgischen Universitätsklinik Heidelberg unter der Leitung des Ärztlichen Direktors, Prof. Dr. Sandro Krieg, einen Tumor entnommen hat, wird dieser im Labor in einzelne Zellen zerlegt. Diese fügen sich in einer Nährflüssigkeit wieder zusammen und bilden Mini-Tumoren, was rund drei Tage dauert. Dann wird das Medikament zugegeben und nach wiederum drei Tagen liegt das Ergebnis vor, ob es gelungen ist, den Mini-Tumor wirksam zu bekämpfen.
Größte Organoid-Kohorte in Meningeomen berücksichtigt Tumor-Unterschiede
Auf diese Weise überprüfte das Forscherteam die neun Inhibitoren an Organoiden, deren Zellen aus Tumoren von 60 an einem Meningeom erkrankten Menschen stammten. „Wir haben damit die bislang größte untersuchte Organoid-Kohorte in dieser Tumor-Entität eingesetzt, um möglichst breit die Heterogenität abzudecken, also verschiedene histologische und molekular Merkmale oder auch unterschiedlich aggressive Formen“, unterstreicht Dr. Gerhard Jungwirth, Erstautor der Studie.
Dieser Aufwand hat sich gelohnt: Im Histon-Deacetylasen-Inhibitor „Panobinostat“ fanden die Forschenden ein Medikament, das offenbar bei einem Großteil der getesteten Organoide eine wirksame Konzentration erreichte. Histon-Deacetylasen sind spezielle Enzyme in menschlichen Zellen. Die als „HDACs“ abgekürzten Biokatalysatoren beeinflussen zusammen mit anderen Eiweißen, welche Bereiche der DNA aktiviert werden. Der HDAC-Inhibitor Panobinostat verhindert, dass Tumorzellen sich vermehren und bekämpft damit das Meningeom. Der Wirkstoff wurde bereits kombiniert mit anderen Medikamenten zugelassen für die Behandlung des Multiplen Myeloms, einer bösartigen Erkrankung des blutbildenden Knochenmarks. Panobinostat sehen die Autorinnen und Autoren der Studie daher als möglichen Therapie-Ansatz, der weiter überprüft und bewertet werden sollte.
Resistenz wie auch Gegenmechanismus beschrieben
Den Autorinnen und Autoren der Studie gelangen noch zwei weiterführende Schritte. Einerseits beschreiben die Forschenden, wie Mini-Tumoren im Verlauf resistent gegen Panobinostat wurden – das Medikament verlor seine Wirksamkeit. Sie überprüften resistente Proben und stellten fest, dass dort das Enzym HDAC8 sowie bestimmte Signalwege verstärkt waren. Wurde HDAC8 herunterreguliert, wurde Panobinostat wirksamer – eine Resistenz ließ sich abwenden.
Originalpublikation
Gerhard Jungwirth et al., Drug screening on tumor organoids exposes therapeutic vulnerabilities of meningiomas to HDAC1/2i panobinostat. Sci. Transl. Med.18, eaea3115(2026).
DOI:10.1126/scitranslmed.aea3115
Kontakt
Prof. Dr. Christel Herold-Mende
Leitung Sektion Experimentelle Neurochirurgische Forschung
Universitätsklinikum Heidelberg
Tel.: 06221 56-6999
Christel.Herold-Mende@med.uni-heidelberg.de