Risk of recurrence in meningiomas: Not only tumor cells, but also their “neighbors” are taken into account in molecular classification.
Scientists at Heidelberg University’s Medical Faculty, the German Cancer Research Center, and the National Center for Tumor Diseases (NCT) in Heidelberg have shown that the molecular classification of brain tumors using artificial intelligence can be significantly influenced by the microenvironment in the tumor—in particular, the immune cells that have migrated there. Classic tissue assessment by staining specific immune cell markers therefore provides a quick and accurate preview of the tumor grade. The results have been published in the journal Nature Genetics.
Full Text in German below.
Rückfallrisiko bei Meningeomen: Nicht nur Tumorzellen, auch ihre „Nachbarn“ zählen bei der molekularen Klassifizierung mit
Wissenschaftlerinnen und Wissenschaftler der Medizinischen Fakultät Heidelberg der Universität Heidelberg, des Deutschen Krebsforschungszentrums und des Nationalen Centrums für Tumorerkrankungen (NCT) Heidelberg haben gezeigt, dass die molekulare Klassifizierung von Hirntumoren durch Künstliche Intelligenz wesentlich durch das Mikromilieu im Tumor – insbesondere die eingewanderten Immunzellen – beeinflusst werden kann. Die klassische Gewebebeurteilung durch Anfärbung bestimmter Immunzellmarker gibt daher eine schnelle und präzise Vorschau auf den Tumorgrad. Die Ergebnisse sind aktuell im Fachjournal „Nature Genetics“ erschienen.
Hirntumoren werden zunehmend anhand molekularer Marker charakterisiert und in Risikogruppen eingeteilt. Dabei spielt die Analyse bestimmter chemischer Veränderungen des Tumorerbguts, sogenannter DNA-Methylierungen, mithilfe Künstlicher Intelligenz (KI) eine wichtige Rolle. Wissenschaftlerinnen und Wissenschaftler der Medizinischen Fakultät Heidelberg der Universität Heidelberg, des Deutschen Krebsforschungszentrums und des Nationalen Centrums für Tumorerkrankungen (NCT) Heidelberg haben nun bei Meningeomen, den häufigsten primären Hirntumoren bei Erwachsenen, gezeigt, dass die KI-erstellte Klassifizierung nicht nur auf den Eigenschaften der Tumorzellen fußt. Auch die Immunzellen, die in das Tumorgewebe eingewandert sind, prägen maßgeblich das molekulare Profil – und geben Aufschluss über die Prognose.
„Es ist umstritten, welche Unterteilung in Subgruppen bei Meningeomen sinnvoll ist, um daraus Behandlungsempfehlungen abzuleiten. Frühere Arbeiten zur Rolle der Methylierung kamen zu unterschiedlichen Ergebnissen“, sagt Felix Sahm, Professor für „Neuropathologie“ an der Medizinischen Fakultät Heidelberg der Universität Heidelberg. „Unsere Arbeit zeigt, dass die Methylierungs-Signale der Immunzellen im Tumor mindestens ebenso wichtige Marker für die KI-Klassifikation sind wie die der Tumorzellen.“
Der Hintergrund: Wird ein Tumor anhand der DNA-Methylierung klassifiziert, erhält die KI die Methylierungsdaten eines Gemischs verschiedener Zelltypen aus dem Tumor, die sie nicht unterscheidet. Durch Training hat die KI gelernt, Muster aus charakteristischen Signalen der gesamten Gewebeprobe bestimmten Risikogruppen zuzuordnen. Wie sich nun herausgestellt hat, sind diese Muster wesentlich von den Immunzellen abhängig. Diese Erkenntnis macht die KI-Klassifizierung und die unterschiedlichen Ergebnisse in früheren Arbeiten bei Meningeomen besser nachvollziehbar.
Im Fokus der Wissenschaftlerinnen und Wissenschaftler standen Meningeome mit Veränderungen im sogenannten NF2-Gen, das den Bauplan für ein Protein zur Kontrolle der Zellteilung enthält. Aus der Analyse umfangreicher Forschungsdatensätze weiß man, dass ein Defekt des NF2-Gens dazu führt, dass diese Regulation entfällt und sich die Tumorzellen unkontrolliert vermehren können. Bei rund der Hälfte aller Meningeome ist das NF2-Gen im Tumorgewebe verändert. Dies lässt allerdings noch keine Vorhersage zu Tumorgrad und Aggressivität zu.
Das Team erstellte mithilfe von KI-gestützten Einzelzellanalysen räumlich aufgelöste Muster der Genaktivität im Tumorgewebe sowie Methylierungsprofile: Bei NF2-bedingten Meningeomen haben Immunzellen, die sich in und um den Tumor sammeln, anscheinend einen Einfluss auf den Krankheitsverlauf. Fanden sich dort überwiegend Immunzellen, die den hirneigenen Mikroglia-Zellen ähnelten, ging dies mit einem geringen Rückfallrisiko und guter Prognose einher. Waren dagegen mehr Makrophagen, Immunzellen aus dem Blut, eingewandert, war der Tumor aggressiver. Denn diese „Fresszellen“, die eigentlich den Körper vor Krankheitserregern schützen sollen, können in einen Modus wechseln, in dem sie den Tumor in seinem Wachstum fördern, anstatt ihn zu bekämpfen.
„Wir wissen jetzt: Es gibt in der Zusammensetzung des Tumor-Mikromilieus keine starren Untergruppen, sondern fließende Übergänge entlang eines Risikospektrums. Die Art der Immunzellen kennzeichnet darin die aktuelle Positionierung des jeweiligen Tumors in diesem Spektrum, die sich aber verändern kann“, so Prof. Dr. Dr. Felix Sahm, der auch als Wissenschaftler am DKFZ und im Deutschen Konsortium für Translationale Krebsforschung (DKTK) tätig ist.
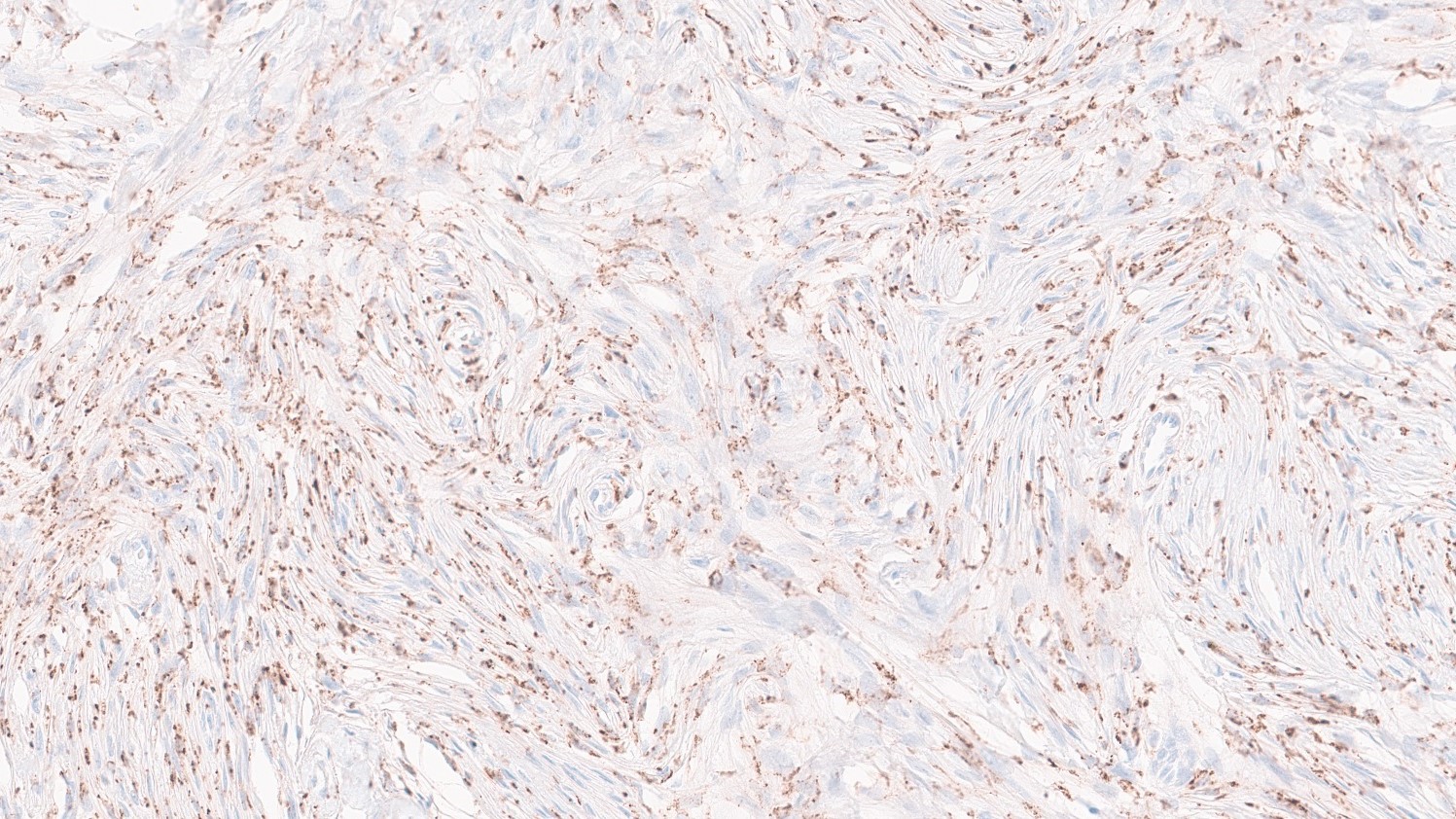
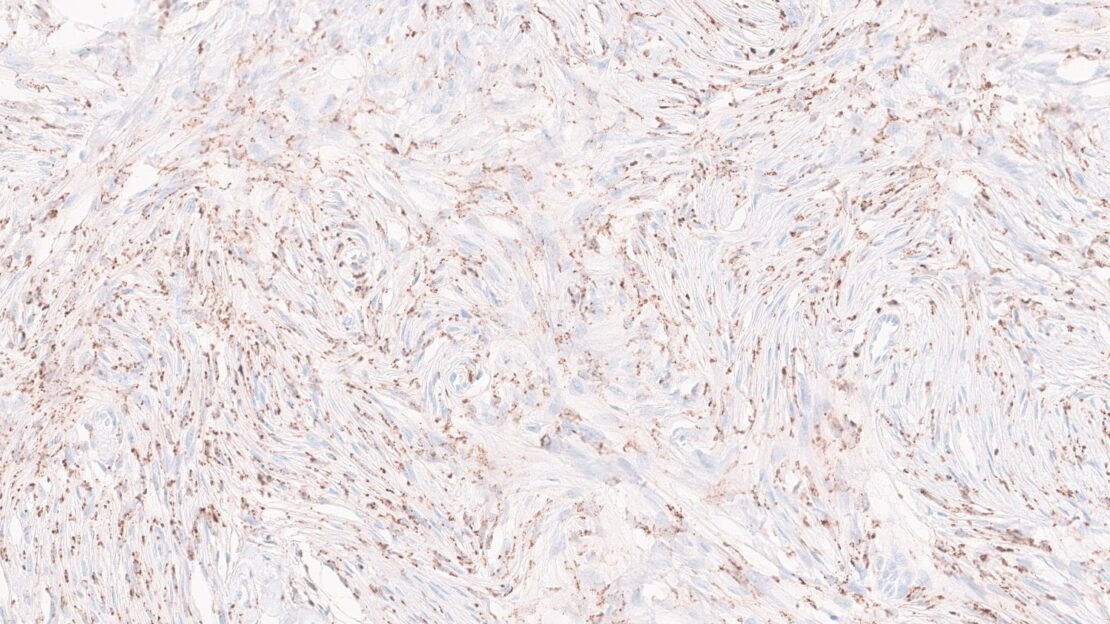
Aus dieser Erkenntnis leiten die Forschenden einen einfachen immunhistochemischen Ansatz ab: Mit Färbetechniken für Makrophagen-Marker (CD68/PU.1) lässt sich ohne großen technischen Aufwand die Anzahl der tumorfördernden Makrophagen im Tumorgewebe abschätzen und so sehr schnell zwischen gut- und bösartigen Tumoren unterscheiden – auch in ressourcenbegrenzten Kliniken ohne Zugang zu modernen Analyselaboren. Zudem hilft die Färbung, die aussagekräftigsten Tumorareale für weiterführende molekulare Tests zu wählen. „Im Prinzip sind wir den Umweg über die KI-basierte molekulare Analyse gegangen, um jetzt zu wissen, welche Basisinformationen wir für eine Risikoabschätzung verwenden können“, so Prof. Dr. Dr. Felix Sahm, stellvertretender Ärztlicher Direktor der Abteilung Neuropathologie und Leiter der Sektion „Molekulare Neuropathologie“ am Universitätsklinikum Heidelberg (UKHD).
Literatur
Maas, S.L.N., Tang, Y., Stutheit-Zhao, E. et al. A microenvironment-determined risk continuum refines subtyping in meningioma and reveals determinants of machine learning-based tumor classification. Nat Genet (2026). https://doi.org/10.1038/s41588-025-02475-w
Weitere Informationen im Internet
Sektion Molekulare Neuropathologie des UKHD
Kontakt
Prof. Dr. Dr. Felix Sahm, MBA
Medizinische Fakultät Heidelberg der Universität Heidelberg
und
Abteilung Neuropathologie, Universitätsklinikum Heidelberg
Tel.: 06221 56-4075
felix.sahm@med.uni-heidelberg.de